SISTEMAS MATERIALES
Materia: Todo lo que ocupa un lugar en el espacio.
Propiedades de la materia: extensivas e intensivas:
- Las propiedades extensivas dependen de la cantidad de materia que se tome para su estudio.
- Las propiedades intensivas son las que son independientes de la cantidad de materia considerada.
Existen tres estados de agregación de la materia:
SOLIDO
LÍQUIDO
GASEOSO
Cambios de estado.
Los cambios de estado son transformaciones físicas en las cuales la materia cambia de estado de agregación, mediante una transferencia o intercambio de energía (calor). Durante dichas transformaciones, la temperatura del sistema permanece constante, denominándose Punto de Fusión, Punto de Ebullición, etc.
A los cambios de estado que se producen por absorción de calor se los denomina cambios progresivos. A los que se producen con desprendimiento de calor se los denomina regresivos.
SISTEMAS MATERIALES
Se llama sistema material a la porción del universo que se elige para su observación y estudio.
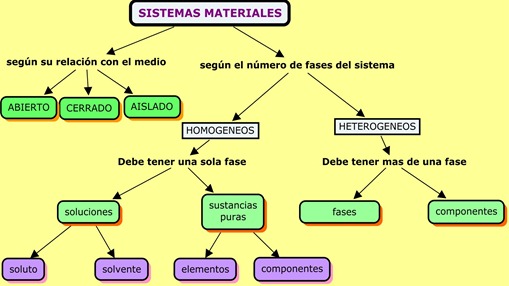
- Se clasifican en sistemas materiales homogéneos y heterogéneos según sus fases.
- Los homogéneos son aquellos que presentan las mismas propiedades intensivas en todos sus puntos, es decir, en cualquier porción del sistema.Debe tener una fase. De acuerdo a su composición, se clasifican en sustancias puras y soluciones.
- Sustancias puras Simples: Son aquellas que no pueden ser separadas en otras sustancias. Ejemplo: Hidrógeno, Azufre, Oxígeno, etc.
- Sustancias Puras Compuestas: Son aquellas que pueden originar a través de reacciones de descomposición, sustancias puras simples. Ejemplo: Dióxido de Carbono, el agua (H2O), etc.
Soluciones: Son sistemas homogéneos formados por dos o más sustancias puras. El componente que está mayor proporción, generalmente líquido, se denomina Solvente o Disolvente, y el que está en menos proporción Soluto. Si un soluto sólido se disuelve en un solvente líquido, se dice que es soluble, en cambio si el soluto también es líquido entonces se dice que es miscible.



- El heterogéneo es aquel que presenta distintas propiedades intensivas en por lo menos 2 puntos. Tiene dos o más fases.



Existen varios métodos mecánicos para separar las fases de un sistema heterogéneo:
- Solubilización.
- Filtración y Evaporación.
- Decantación.
- Centrifugación.
- Levigación.
- Tamización.
- Sublimación.
-Tría.
- Inmantación.
2. Según el intercambio con el medio ambiente:
- Abiertos: Son aquellos que intercambian materia y energía con el medio ambiente. Por ejemplo: Una pava con agua hirviendo.
- Cerrados: Son aquellos que solo intercambian energía con el medio ambiente. Por ejemplo: una lamparita encendida.
- Aislados: Son aquellos que no intercambian ni materia ni energía con el medio ambiente. Por ejemplo: Un termo cerrado.
No hay comentarios.:
Publicar un comentario